1904 m. Nobelio premija chemijos srityje skirta Viljamui Ramziui (William Ramsay, 1852–1916) už inertinių dujų atradimą. Pirmąsias atrastas inertines dujas jis pavadino argonu (graikiškai argos – „tingus“). Šį pavadinimą argonas pelnė dėl savo cheminio inertiškumo. Beje, visu šimtmečiu anksčiau Henris Kavendišas (Henry Cavendish, 1731–1810) oro mėginį prisotino deguonies ir leido elektros išlydžius. Taip jis privertė azotą jungtis su deguonimi. H. Kavendišas nustatė, kad 1/125 oro tūrio dalis (t. y. 0,8 %) nesijungia nei su azotu, nei su deguonimi ir, tikėtina, yra kažkokios kitos dujos. Dabar nustatyta argono tūrio dalis ore 0,9 %. Tad H. Kavendišas jau buvo aptikęs argoną gerokai anksčiau už V. Ramzį, bet neįrodė, kad tai nauja medžiaga. Kodėl inertinės dujos tokios nereaktyvios? Cheminės reakcijos susijusios su elektroninės sandaros pokyčiais. Tad inertiškumo priežastis gali būti inertinių dujų elektroninės sandaros ypatumai – jos turi visiškai užpildytas išorinio sluoksnio s ir p orbitales – vadinamąjį elektronų oktetą (helis turi užpildytą s orbitalę). Elektronų okteto idėja pasitarnavo aiškinant cheminio ryšio susidarymą – atomai atiduoda, prisijungia arba bendrina elektronus ir taip įgyja sandarą, panašią į inertinių dujų.
Beje, inertinės dujos ne visai inertinės. Jau senokai pavyko susintetinti kriptono, ksenono junginius, o 2000-aisiais metais paskelbta apie argono junginį HArF, tiesa, egzistuojantį tik žemesnėje nei –256 °C temperatūroje.
Išnagrinėję šį skyrių, gebėsite:
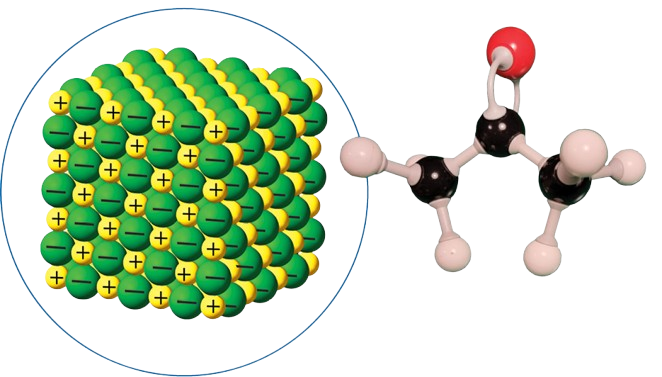
- paaiškinti joninių junginių susidarymą;
- nusakyti joninio kristalo sandarą ir savybes;
- paaiškinti kovalentinio ryšio susidarymą;
- nurodyti kovalentinio nepolinio ir kovalentinio polinio ryšio skirtumus;
- išvardyti nemolekulinės sandaros kovalentinių junginių sandaros ypatumus;
- palyginti skirtingais cheminiais ryšiais susijusių medžiagų savybes;
- paaiškinti cheminio ryšio susidarymą koordinaciniu būdu; nustatyti metališkojo ryšio susidarymą ir savybes;
- paaiškinti tarpmolekulinio ryšio susidarymą;
- nusakyti tarpmolekulinio ryšio įtaką medžiagų savybėms;
- pateikti vandenilinio ryšio susidarymo biologiškai svarbiose medžiagose pavyzdžių.
