Žinios apie atomo sandarą ilgus amžius rinktos po kruopelytę. Visą žinomą informacijos apie atomą kaupimo laikotarpį santykinai galima suskirstyti į tris toliau aptariamus etapus.
Nuo Demokrito iki Dž. Doltono
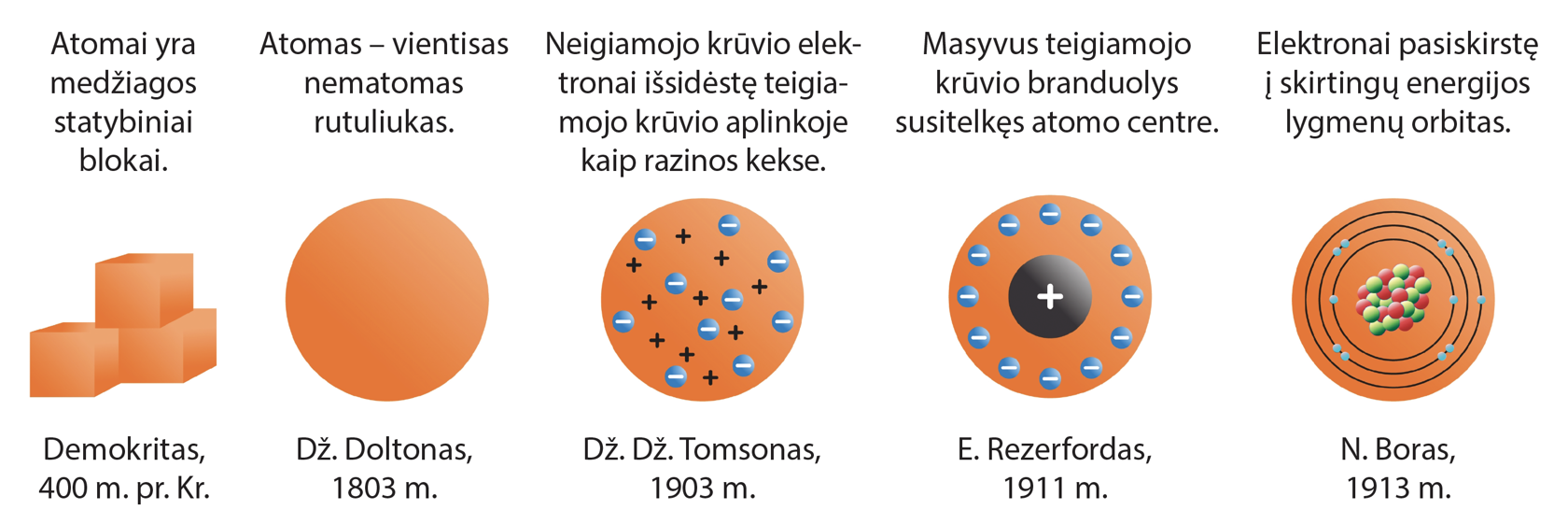
Remiantis jau minėto Demokrito idėjomis, buvo manoma, kad atomai yra nedalios kietosios dalelės, jų deriniai sudaro įvairius kūnus, o atomų judėjimas lemiąs visus tuose kūnuose vykstančius réiškinius. XVIII a. pabaigoje anglų chemikas Džonas Doltonas (John Dalton, 1766–1844) (6.3.1 pav.) atomą ėmėsi nagrinėti kaip mažiausią cheminio elemento dalelę. Jo teigimu, cheminiai elementai vienas nuo kito skiriasi atomų mase.

Esminiai Dž. Doltono teorijos teiginiai:
- kiekvienas cheminis elementas yra sudarytas iš mažų dalelių – atomų;
- atomai yra nematomi, jų negalima sukurti ar sunaikinti;
- visi to paties cheminio elemento atomai yra vienodi;
- medžiagos susidaro jungiantis skirtingų cheminių elementų atomams.
XIX a. pabaiga – XX a. pradžia
1897 m. atradus elektroną, galutinai paaiškėjo, kad atomas sudarytas iš dar mažesnių dalelių. Vėliau sùprasta, kad atomo sandara gerokai sudėtingesnė. 1903 m. britų fiziko Džozefo Džono Tomsono (Joseph John Thomson, 1856–1940) (6.3.2 pav.) pasiūlytame modelyje atomas yra mažas rutuliukas. Atome (rutuliuke) teigiamojo krūvio aplinkoje išsidėstę neigiamojo krūvio elektronai – kaip razinos kekse. Elektronų bendras neigiamasis krūvis lygus teigiamajam rutuliuko krūviui. Dž. Dž. Tomsono modelis buvo pažangesnis už ankstesnius – jame numatyta, kad atome yra elektronų, bet fizikai, remdamiesi šiuo modeliu, dar negalėjo paaiškinti daugelio reiškinių.

1911 m. škotų išeivio iš Naujõsios Zelándijos sūnus Ernestas Rezerfordas (Ernest Rutherford, 1871–1937) (6.3.3 pav.) įrodė, kad teigiamasis krūvis nėra pasiskirstęs po visą atomą tolygiai, o sutelktas itin mažame tūryje – atomo branduolyje. Anot jo, elektronai skrieja aplink branduolį lyg planetos aplink Saulę, o neutralaus atomo elektronų skaičius toks, kad jų bendras neigiamasis krūvis lygus teigiamajam branduolio krūviui.

Tolesnis žinių apie atomą kaupimo etapas siejamas su moderniąja fizika ir N. Boro pavarde. Atomo modelio raida pavaizduota 6.3.4 paveiksle. Atomo modelis tobulinamas iki šiol.
Platesniam akiračiui
Moderniosios fizikos etapas
Šį etapą pradėjo jau minėtas N. Boras (6.3.5 pav.), subūręs jaunus mokslininkus. Prasiskverbti į atomo paslapčių gelmes buvo ypač sunku: mikropasaulio taisyklės nuo mums suprantamų skyrėsi iš esmės. Amžiais kurtą įprastų vaizdinių kalbą reikėjo keisti nauja. 6.1 lentelėje pateikti teiginiai, iliustruojantys esminius mums įprasto pasaulio ir mikropasaulio skirtumus.

6.1 lentelė. Mums įprasto pasaulio ir mikropasaulio palyginimas
Mums įprastas pasaulis – makropasaulis | Mikropasaulis |
Objektai – akmuo, dviratis, Mėnulis. | Objektai – elektronai ar kitos mikropasaulio dalelės. |
Vienu metu objektas gali judėti viena trajektorija; ją galima stebėti. | Iš vieno taško į kitą elektronas gali judėti visomis galimomis trajektorijomis; jų užfiksuoti neįmanoma. |
Tuo pačiu metu galima fiksuoti objekto padėtį erdvėje ir jo greitį. | Elektrono padėties erdvėje ir greičio matavimų tuo pačiu metu atlikti neįmanoma! |
Galioja priežastingumas: žinant, kas yra dabar, galima nuspėti, kas bus toliau. | Tolesnio vyksmo nuspėti neįmanoma – jis atsitiktinis. |
Matuojant objekto būseną, pats objektas nesikeičia: pvz., išmatavome stalviršio ilgį, stalas nepakito. | Neįmanoma išmatuoti elektrono būsenos, jos nepakeitus: vien tik stebint elektroną, jo būsena – greitis, padėtis – kinta. |
Dž. Doltonui buvo būdingas savotiškas bruožas eikvoti mokslininko entuziazmą objektyviai neįveikiamoms temoms. Jis taip domėjosi meteorologiniais reiškiniais, kad, nepaisydamas fakto, jog neskiria spalvų, aprašė... šiaurės pašvaistę. Ji Dž. Doltono vaizduotėje virto „elastingu skysčiu, įgavusiu cilindrinių spindulių formą“.
Klausimai ir užduotys
- Įvardykite tris esminius Dž. Doltono teiginius apie atomą.
- Prisiminkite, kokias medžiagų savybes vadiname cheminėmis, kokias – fizikinėmis.
- Įvardykite mažiausią cheminio elemento dalelę ir mažiausią medžiagos dalelę.
- Palyginkite Demokrito ir Dž. Doltono teiginius – įvardykite jų panašumus ir skirtumus.
- Kuo iš esmės skyrėsi Dž. Dž. Tomsono ir E. Rezerfordo atomo modeliai?
- Kuo mikropasaulio taisyklės skiriasi nuo mums suvokiamo makropasaulio tvarkos? Nurodykite du skirtumus.
- Italų kilmės fizikas Enrikas Fermis (Enrico Fermi, 1901–1954) teigė, kad sąvoką „elementarus“ reikia taikyti ne atomui kaip dalelei apibūdinti, o mūsų žinių apie atomą lygiui. Kaip suprantate šį pasakymą?
- Kada, jūsų nuomone, baigsis atomo modelio kūrimas?
- Ar keičiasi jūsų būsena prieš kontrolinį darbą, svarbų susitikimą, įvykį? Kaip manote, kodėl? Savo atsakymą susiekite su aptariama tema.

