Santykinių masių svertinis vidurkis
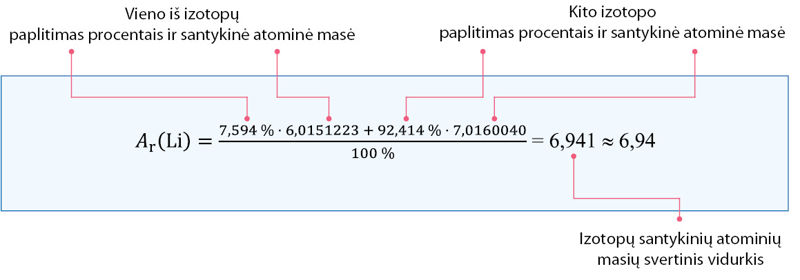
Ištyrus masių spektrometru nustatyta, kad gamtoje aptinkamas litis yra dviejų izotopų mišinys. Tyrimo duomenys pateikti 2.1 lentelėje ir 2.2. temos 2.2.3 paveiksle. Periodinėje lentelėje nurodyta, kad ličio santykinė atominė masė yra 6,94. Šis skaičius nesutampa nei su , nei su
2.1 lentelė. Gamtinių ličio izotopų paplitimas
Izotopas | Santykinė atominė | Paplitimas, % |
6,0151223 | 7,594 | |
7,0160040 | 92,414 |
1 pavyzdys
Gamtinis bromas (2.3.2 pav.) yra dviejų izotopų mišinys (2.2 lentelė).
2.2 lentelė. Gamtinių halogenų izotopų paplitimas
Izotopas | Santykinė atominė | Paplitimas, % |
18,9984032 | 100 | |
34,96885271 | 75,784 | |
36,96590261 | 24,224 | |
78,9183376 | ? | |
80,916291 | ? | |
126,904468 | 100 |
- Nustatykite, kiek protonų ir neutronų turi kiekvienas bromo izotopas.
- Paaiškinkite, ar įmanoma nustatyti bromo neutronų skaičių naudojantis tik periodine lentele.
- Apskaičiuokite bromo izotopų paplitimą procentais.
Sprendimas
- Bet kuris bromo izotopas turi 35 protonus, o neutronų skaičius yra skirtingas.
Br 35 79 Br 35 81 - Periodinėje lentelėje nurodytas izotopų santykinių atominių masių vidurkis, o ne konkretaus izotopo masės skaičius, todėl neutronų skaičiaus vien iš periodinės lentelės duomenų nustatyti nepavyks. Skirtingi izotopai turi skirtingą neutronų skaičių, todėl būtina žinoti, kurio izotopo sudėtis domina.
- Kadangi reikia apskaičiuoti dviejų izotopų paplitimą, būtina sudaryti dvi lygtis. Tarkime, kad
Br 35 79 Br 35 81
Atsakymas
x = 50,87 % (
y = 49,13 % (

Kelios pastabos:
- Masės skaičius (vieno ličio izotopo jis yra 6, kito – 7) visada yra sveikasis skaičius, nes jis rodo bendrą protonų ir neutronų skaičių branduolyje. Dalelių skaičius negali būti trupmeninis.
- Izotopo santykinė atominė masė būna trupmeninis skaičius. Tik suapvalinta iki sveikojo skaičiaus ji sutampa su izotopo masės skaičiumi.
- Vienintelio anglies izotopo 12C santykinė atominė masė yra sveikasis skaičius (lygus tiksliai 12), nes šis izotopas pasirinktas etalonu, pagal kurį matuojama kitų atomų santykinė masė.
- Elemento santykinė atominė masė nesutampa su vieno ar kito izotopo santykine mase. Ji apskaičiuojama atsižvelgiant į to elemento izotopų paplitimą gamtoje.
Klausimai ir užduotys
- Mokinio chemijos žinios įvertintos dešimtukais ir aštuntukais. Dešimtukai sudaro 80,0 % jo pažymių, o aštuntukai – 20,0 %. Apskaičiuokite mokinio pažymių svertinį vidurkį. Atsakymą pateikite trimis reikšminiais skaitmenimis. Kuo šio uždavinio sprendimas susijęs su elemento santykinės atominės masės apskaičiavimu?
- Apskaičiuokite chloro santykinę atominę masę. Atsakymą palyginkite su pateiktu skaičiumi periodinėje lentelėje. Naudokitės 2.2 lentelės duomenimis.
- Chloro molekulės formulė Cl2. Molekulės santykinė masė yra ją sudarančių atomų santykinių masių suma. Gamtoje paplitę chloro izotopai nurodyti 2.2 lentelėje. Kiek skirtingų Cl2 molekulių susidaro iš šių izotopų? Kokia kiekvienos šių molekulių santykinė masė (atsakymą pateikite suapvalintą iki trijų reikšminių skaitmenų)? Patarimas: dar kartą išnagrinėkite 2.3.2 paveikslo informaciją.
- Gamtoje aptinkami du vario izotopai: varis-63 (Ar = 62,9296011) ir varis-65 (Ar = 64,9277937). Periodinėje lentelėje nurodyta vario santykinė atominė masė Ar = 63,55.
- Nurodykite, kiek protonų, neutronų ir elektronų turi
Cu 29 63 Cu 2 + 29 65 - Apskaičiuokite vario izotopų paplitimą procentais. Atsakymą suapvalinkite iki trijų reikšminių skaitmenų.
- Nurodykite, kiek protonų, neutronų ir elektronų turi
- Ar tiesa, kad kiekvieno chloro atomo santykinė masė yra 35,4527? Atsakymą paaiškinkite.
