Elektrònų slúoksnis, valeñtinis slúoksnis, valeñtiniai elektrònai, valentingùmas, taškinė elektròninė (Lùiso) fòrmulė, pagrindinis kvántinis skaičius, elektrònų konfigūrãcija.
Elektronų sluoksniai
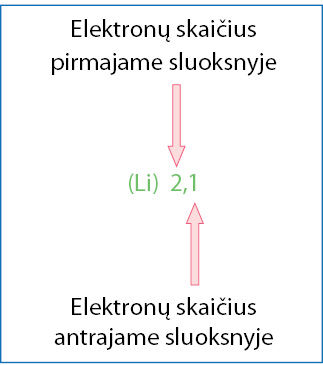
Atomo elektronų išsidėstymas vadinamas jo elektrònų konfigūrãcija. Ličio elektronai išsidėstę dviem sluoksniais. Du mažesnės energijos elektronai skrieja arčiau branduolio, o vienas, didesnės energijos, nutolsta toliau. Sutrumpintai ličio elektronų išsidėstymas užrašomas taip: 2, 1 (2.4.1 pav.).
Toliausiai nuo branduolio esantis elektronų sluoksnis vadinamas valeñtiniu3, o jame esantys elektronai – valeñtiniais elektrònais. Ličio atomas turi vieną valentinį elektroną.
3Lotynų kalba žodis valens reiškia „stiprus, galingas, pajėgus“. Nuo valentinių elektronų skaičiaus priklauso atomo geba jungtis su kitais atomais. Ši geba vadinama valentingumu.
1 pavyzdys
Sieros elektronų pasiskirstymo sluoksniais formulė yra 2, 8, 6. Paaiškinkite, kokias išvadas galima padaryti iš šios formulės.
Sprendimas
Formulėje nurodyti trys skaičiai, vadinasi, sieros elektronai yra išsidėstę trimis sluoksniais. Arčiausiai branduolio esančiame pirmajame sluoksnyje yra du elektronai, antrajame – aštuoni. Trečiasis sluoksnis yra valentinis. Jame yra šeši elektronai.
Pirmųjų dvidešimties elementų elektronų konfigūracija (elektroninė sandara)
Kuo toliau nuo branduolio yra sluoksnis, tuo daugiau jame telpa elektronų.
Didžiausias elektronų skaičius sluoksnyje = 2n2.
(2.4.1)
Raide n pažymėtas sluoksnio numeris (n dar vadinamas pagrindiniù kvántiniu skaičiumi). Pirmuosiuose trijuose sluoksniuose elektronų gali būti ne daugiau kaip:
1-ajame 2 · 12 = 2;
2-ajame 2 · 22 = 8;
3-iajame 2 · 32 = 18;
n-tajame 2n2.
Būtent todėl, kad pirmajame sluoksnyje negali būti daugiau nei du elektronai, pirmajame periode yra tik du elementai – vieną elektroną turintis vandenilis ir du elektronus turintis helis.
Litis turi tris elektronus. Du iš jų yra pirmajame sluoksnyje (2.4.1 pav.). Trečiajam elektronui čia vietos nebėra, todėl atsiranda antrasis sluoksnis. Litis yra pirmasis antrojo periodo elementas, turintis du elektronų sluoksnius. Naujo sluoksnio atsiradimas susijęs su naujo periodo pradžia.
Nuo ličio iki neono elektronų skaičius antrajame sluoksnyje didėja nuo 1 iki 8. Neono atomas turi du visiškai užpildytus sluoksnius ir užbaigia antrąjį periodą. Nuo natrio prasideda trečiasis periodas.
Kai svarbus tik elektronų skaičius valentiniame sluoksnyje, rašomos taškinės elektròninės, arba Lùiso4, fòrmulės. Jos sudaromos prie elemento simbolio dedant valentinius elektronus žyminčius taškus arba kryžiukus. Pirmieji keturi valentiniai elektronai žymimi po vieną, o pradedant nuo penktojo sudaromos elektronų poros (2.3 lentelė).
4 Gilbertas Niutonas Luisas (Gilbert Newton Lewis, 1875–1946) tyrė cheminių ryšių susidarymą ir pasiūlė naudoti taškines elektronines formules.
2.3 lentelė. Pirmųjų 20 elementų taškinės elektroninės (Luiso) formulės
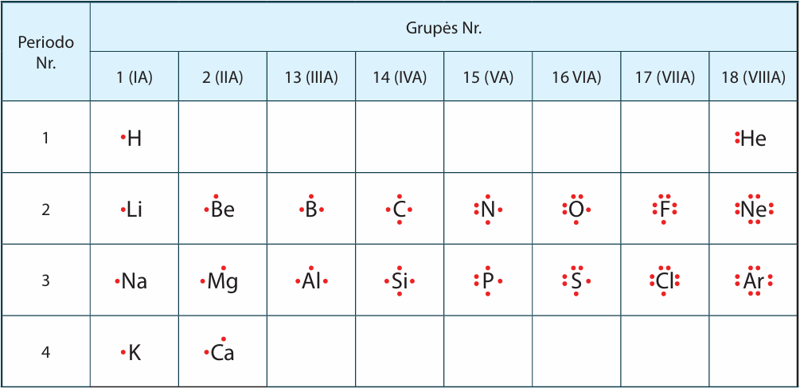
Atkreipkite dėmesį, kad paskutinis trečiojo periodo elementas argonas išoriniame (trečiajame) sluoksnyje turi aštuonis elektronus, nors čia jų gali būti net aštuoniolika. Išoriniame neutralaus atomo sluoksnyje nebūna daugiau kaip aštuoni elektronai. Trečiajame sluoksnyje elektronų pradės gausėti tik pradedant nuo 21-ojo elemento skandžio.
2 pavyzdys
Nurodykite azoto atomo elektronų sluoksnių ir valentinių elektronų skaičių.
Sprendimas
Azotas yra 2-ojo periodo elementas, vadinasi, elektronai yra išsidėstę dviem sluoksniais. Tai 15 grupės elementas, tad valentinių elektronų yra 5.
Komentaras. Jei grupės numeris yra dviženklis skaičius, valentinių elektronų skaičių rodo antrasis skaitmuo. Tradiciškai dar tebenaudojama senesnė grupių numeracija su romėnų skaitmeniu ir raidėmis A arba B. A grupių numeris rodo valentinių elektronų skaičių. Tik helis, nors yra 18, arba VIIIA, grupės elementas, turi tik du valentinius elektronus.
Klausimai ir užduotys
- Iš toliau pateiktų elementų pasiskirstymo sluoksniais formulių nustatykite, kiek elektronų yra kiekviename nurodytų atomų sluoksnyje ir kiek šie atomai turi valentinių elektronų:
- (F) 2, 7;
- (Al) 2, 8, 3;
- (Ca) 2, 8, 8, 2.
- Antrasis periodas baigiasi neonu, turinčiu du elektronų sluoksnius. Apskaičiuokite, kiek daugiausia elektronų gali būti antrajame sluoksnyje, ir nustatykite, ar šis neono atomo sluoksnis jau užpildytas.
- Sudarykite elektronų pasiskirstymo sluoksniais ir Luiso elektronines formules, naudodamiesi tik užduotyje pateikta informacija ir formule 2n2:
- silicis yra 3-iojo periodo 14-osios grupės elementas;
- fosforas yra 3-iojo periodo 15-osios grupės elementas.
- Kuri iš elektronų pasiskirstymo sluoksniais formulių neteisinga? Atsakymą paaiškinkite.
- 2, 3
- 2, 8, 1
- 2, 9, 2
- 2, 8, 8
- Nežinomo elemento elektronų pasiskirstymo sluoksniais formulė yra x, y, 7. Kam lygūs skaičiai x ir y? Kaip vadinasi nežinomas elementas?

