Skyriaus santrauka
- Cheminiai elementai yra paprastosios medžiagos, iš kurių sudarytos visos kitos medžiagos.
- Cheminiais kitimais elementų negalima suskaidyti į mažesnes dalis.
- Visi žinomi cheminiai elementai yra surašyti į periodinę cheminių elementų lentelę.
- Tarp cheminių elementų daugiausia yra metalų, gerokai mažiau – nemetalų ir visai nedaug – pusmetalių.
- Cheminio elemento atomą sudaro branduolys ir elektronai.
- Atomo branduolį sudaro teigiamąjį krūvį turintys protonai ir krūvio neturintys neutronai.
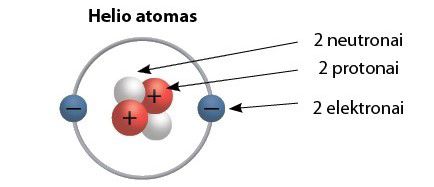
- Elemento eilės numeris (atominis skaičius) reiškia protonų skaičių to elemento atomo branduolyje.
- Branduolį sudarančių protonų ir neutronų skaičius gali skirtis.
- Protonų ir neutronų masių suma vadinama masės skaičiumi.
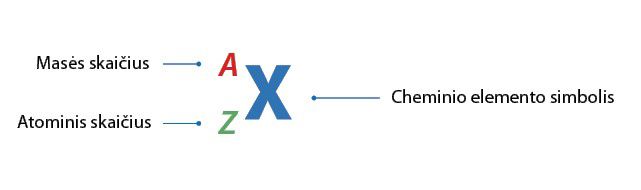
- Atomo protonų skaičius visada lygus neigiamąjį krūvį turinčių elektronų skaičiui.
- Elektronai beveik 2000 kartų lengvesni už protonus.
- Atomai, kurie turi tą patį protonų skaičių, bet skirtingą neutronų skaičių, vadinami izotopais.
- Elemento izotopų atominis skaičius sutampa, skiriasi tik masės skaičius.
- Atominiu masės vienetu pasirinkta
$\frac{1}{12}$112 stabilaus anglies izotopo 12C masės. - Apskaičiuojant cheminio elemento santykinę atominę masę vertinama to elemento izotopų masė ir paplitimas.
- Periodinę cheminių elementų lentelę sudaro grupės ir periodai.
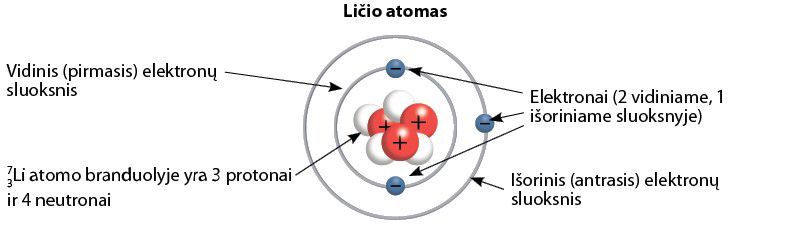
- Periodo numeris atspindi elemento atomo elektronų sluoksnių skaičių.
- Atomų elektronų sluoksniai, esantys arčiau branduolio, vadinami vidiniais. Sluoksnis, pildomas elektronais, yra išorinis. Jei išoriniame elektronų sluoksnyje daugiau elektronų nebegali būti, šis sluoksnis laikomas užpildytu.
- Atomai, turintys visiškai užpildytą išorinį elektronų sluoksnį, yra stabilesni.
- Pirmojo periodo elementų atomų išorinis sluoksnis yra užpildytas tada, kai jame yra du elektronai, antrojo ir trečiojo periodo elementų – tada, kai jame yra 8 elektronai.
- Grupės numeris atspindi elektronų skaičių išoriniame elektronų sluoksnyje.
- Vienos grupės elementai turi panašių savybių. Tai lemia jų atomų išorinio elektronų sluoksnio sandara.
- Gebėjimas lengvai atiduoti išorinio sluoksnio elektroną būdinga pirmosios grupės elementų savybė. Atidavę elektroną jie virsta teigiamaisiais jonais.
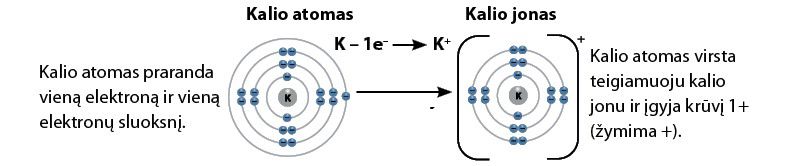
- Halogenai, kuriems iki išorinio elektronų sluoksnio užpildymo trūksta 1 elektrono, yra labai aktyvūs ir linkę prisijungti elektroną. Prisijungę elektroną, jie virsta neigiamaisiais jonais.
- Atomo spindulys yra atstumas nuo atomo branduolio iki to atomo tolimiausio elektronų sluoksnio. Perioduose atomo spindulys mažėja einant iš kairės į dešinę.
- Atomo spindulys grupėse didėja iš viršaus į apačią. Didėjant atomo spinduliui, elektronai prie branduolio traukiami silpniau.
Pasitikrinu ir įsivertinu
- Toliau pateikti elementų simboliai. Parašykite kiekvieno elemento pavadinimą ir nurodykite, kas tai: metalas, nemetalas ar pusmetalis.
- Li
- B
- N
- Al
- Si
- P
- S
- Kurioje elementų grupėje metalų yra daugiau nei nemetalų?
- VIIA
- VIA
- VA
- IVA
- Naudodamiesi periodine cheminių elementų lentele, atlikite toliau pateiktas užduotis.
- Silicio masės skaičius 28, jo atomas turi 14 elektronų. Nurodykite, koks yra šio elemento cheminis simbolis, atominis skaičius, protonų ir neutronų skaičius.
- Cheminio elemento simbolis yra N. Jo atomo branduolyje yra 7 neutronai. Nurodykite šio cheminio elemento pavadinimą, atominį skaičių, masės skaičių, protonų ir elektronų skaičių.
- Cheminio elemento atominis skaičius yra 17, o jo masės skaičius – 35. Nurodykite šio elemento pavadinimą, simbolį, protonų, neutronų ir elektronų skaičių.
- Cheminio elemento branduolyje yra 13 protonų ir 14 neutronų. Nurodykite šio elemento pavadinimą, simbolį, atominį skaičių, masės skaičių ir elektronų skaičių.
- Kurio iš šių atomų branduolyje yra 12 neutronų?
- 25Mg
- 23Na
- 27Al
- 31P
- Gamtoje aptinkami trys magnio izotopai. Jų masės skaičius ir paplitimas (izotopo masės dalis gamtinio elemento sudėtyje) pateikti lentelėje. Remdamiesi šia lentele, nustatykite magnio santykinę atominę masę, skaičiuodami trijų reikšminių skaitmenų tikslumu.
Izotopas | Paplitimas, % | Izotopo santykinė atominė masė |
24Mg | 79,0 | 23,985 |
25Mg | 10,0 | 24,985 |
26Mg | 11,0 | 25,982 |
- Nustatykite, kiek protonų, neutronų ir elektronų turi pateiktų cheminių elementų izotopai:
- 54Fe;
- 57Fe;
- 79Br;
- 81Br.
- Nupieškite aliuminio atomo elektronų išsidėstymą sluoksniais. Kodėl šis elementas priskiriamas IIIA grupei?
- Kuriame grafike tinkamai pavaizduota atomų išorinio sluoksnio elektronų skaičiaus priklausomybė nuo protonų skaičiaus?

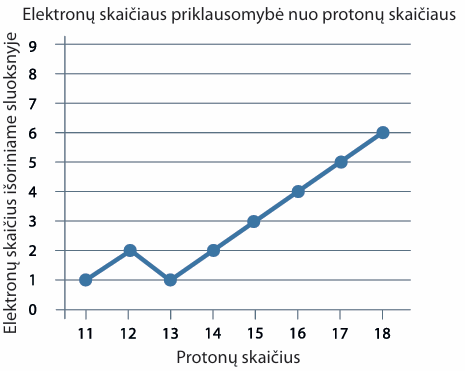
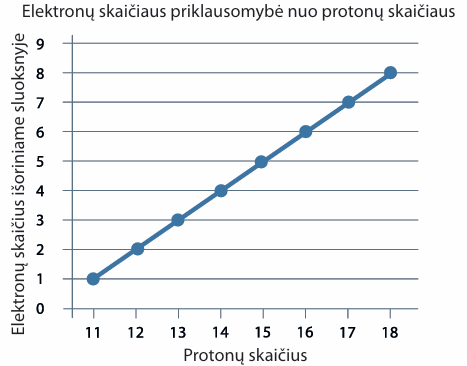
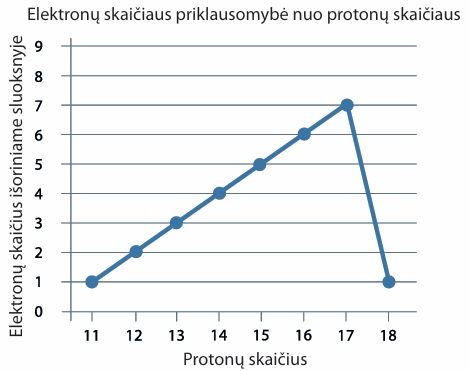
- Naudodamiesi periodine cheminių elementų lentele, pagal toliau pateiktus apibūdinimus nustatykite, kokie tai cheminiai elementai:
- 2 periodo IIA grupės elementas;
- elementas, kurio atominis skaičius 14;
- 3 periodo elementas, kurio santykinė atominė masė 31.
- Kurio elemento branduolyje yra 2 protonai ir 2 neutronai?
- Panagrinėkite toliau pateiktus cheminių elementų atomų modelius ir nurodykite, kuris elementas kuriame paveiksle pavaizduotas.
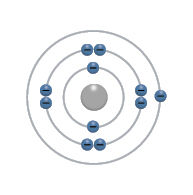
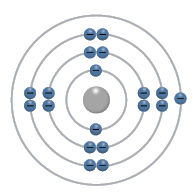
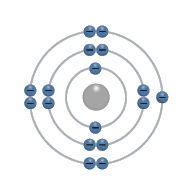
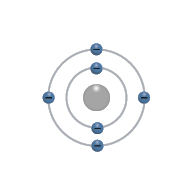
- Pavaizduokite cheminio elemento boro atomo modelį (branduolį sudarančius protonus ir neutronus, elektronų sluoksnius ir juose išsidėsčiusius elektronus).
- Periodinėje cheminių elementų lentelėje raskite cheminius elementus, kuriems suteiktas žemyno ar valstybės pavadinimas. Užrašykite elemento simbolį, šalia jo – žemyno ar valstybės pavadinimą. Kuris iš šių elementų sunkiausias? Kuris iš jų turi mažiausiai elektronų?
- Pasiskirstykite į dvi grupes. Toliau išvardytas sąvokas surašykite ant atskirų lapelių, lapelius sulankstykite, kad nematytumėte užrašo. Kiekviena grupė turi ištraukti po 8 lapelius. Turite kuo vaizdingiau paaiškinti kitai grupei kiekvieną jums atitekusią sąvoką, neištardami šios sąvokos reikšminių žodžių. Laimi komanda, atspėjusi daugiau sąvokų. Sąvokos: protonas, elektronas, neutronas, jonas, atomas, izotopas, joninis ryšys, elektrinis neigiamumas, stabilus atomas, elektronų sluoksnis, branduolys, inertinės dujos, halogenai, metalai, nemetalai, pusmetaliai.
Šią užduotį galite atlikti ir poromis.
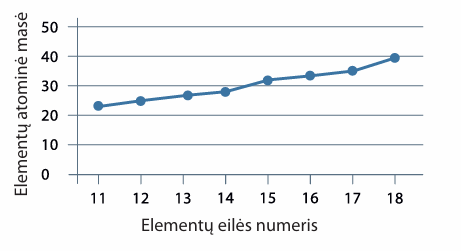
- Toliau pateiktame grafike pavaizduotas vieno periodinės elementų lentelės periodo elementų atominės masės kitimas augant jų eilės numeriui. Nurodykite, koks tai periodas. Nustatykite šių elementų atomų pagrindinių izotopų branduolių sudėtį. Tuo atveju, jei to neįmanoma padaryti, paaiškinkite, kodėl.
Elementų atominės masės kitimo augant jų eilės numeriui grafikas