Tirpiklis, tirpinỹs, tirpalas, mãsės dalis, procentinė koncentrãcija, mãsės koncentrãcija, mòlinė koncentrãcija, tañkis.
Masės ir molinė koncentracija
Tirpalo sudėčiai apibūdinti nurodoma tirpinio:
- mãsės dalis procentais – ω (procentinė koncentracija, žr. 1.3. temą);
- mãsės koncentrãcija – cω , kuria rodoma tirpinio masė pasirinktame tūryje (pvz., 1 dm3, 1 l, 1 cm3, 1 ml);
- mòlinė koncentrãcija – c, kuria rodomas tirpinio kiekis moliais viename kubiniame decimetre (t. y. litre) tirpalo.
Atlikdami su tirpinio koncentracija susijusius skaičiavimus galime sudaryti proporcijas arba taikyti formules:
(1.5.1)
(1.5.2)
1 pavyzdys
Į stiklinę arbatos įdėti ir ištirpinti 3 arbatiniai šaukšteliai cukraus. Žinoma, kad vieno arbatinio šaukštelio cukraus masė 5,0 g, o stiklinės tūris 0,20 l, arba 0,20 dm3. Cukraus cheminė formulė C12H22O11. Apskaičiuokite šiame tirpale esančio cukraus:
- masės koncentraciją;
- molinę koncentraciją.
Sprendimas
- Ištirpinto cukraus masė m = 5,0 g · 3 = 15 g.
Tirpalo tūris V = 0,20 dm3.
- Masės koncentracija rodo, kad viename kubiniame decimetre (t. y. litre) tirpalo yra 75 g cukraus. Dabar lieka tik perskaičiuoti cukraus masę į kiekį moliais.
M(C12H22O11) = 342,34 g/mol;
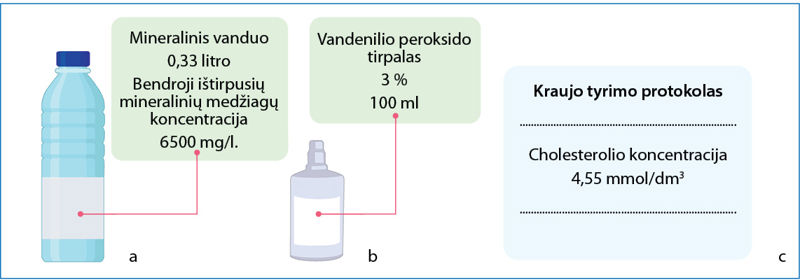
Komentaras. Abiem atvejais kalbama apie tą patį tirpalą, tik koncentracija išreiškiama skirtingais matais: vienam kubiniam decimetrui (litrui) tirpalo a) atveju tenka 75 g, b) atveju – 0,22 mol cukraus. Pirmasis koncentracijos reiškimo būdas labiau paplitęs buityje, antrasis – laboratorijose (1.5.1 pav., p. 24).
Atsakymas: cukraus masės koncentracija 75 g/dm3, o molinė koncentracija 0,22 mol/dm3.
Tankio ir masės koncentracijos matai gali būti painiojami. Abiem atvejais nurodomas masės ir tūrio santykis, tačiau skirtingų objektų. Pavyzdžiui, tirpalo tankis 1,5 g/cm3 rodo, kad vieno kubinio centimetro tirpalo masė yra 1,5 g (masė ir tūris to paties tirpalo), o cukraus koncentracija 0,075 g/cm3 reiškia, kad viename kubiniame centimetre tirpalo yra 0,075 g cukraus (masė cukraus, o tūris tirpalo). Būkite atidūs skaitydami tekstą.
2 pavyzdys
Ankstesniame pavyzdyje aprašytas tūrio matavimas stiklinėmis arba masės nustatymas šaukšteliais yra tik apytikslis. Kai reikia didesnio tikslumo, naudojamasi svarstyklėmis ir matavimo kolbomis. Sudarykite planą, kaip reikėtų pagaminti 100,0 cm3 0,15 mol/dm3 vario(II) sulfato CuSO4 tirpalo, jeigu laboratorijoje turimas vario(II) sulfato kristalohidratas CuSO4 · 5H2O.
Sprendimas
Viename molyje CuSO4 · 5H2O yra vienas molis CuSO4, tad kristalohidrato reikės irgi 0,015 mol.
M(CuSO4 · 5H2O) = 249,72 g/mol;
m(CuSo4 · 5H2O) = n · M = 0,015 mol · 249,72 g/mol = 3,7458 g ≈ 3,75 g.
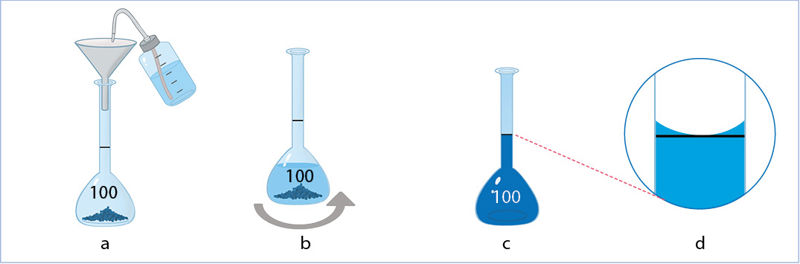
Pasveriama 3,75 g CuSO4 · 5H2O ir daroma taip, kaip aprašyta 1.5.2 paveiksle.
3 pavyzdys
Apskaičiuokite gliukozės C6H12O6 masės ir procentinę koncentraciją tirpale, jei šios medžiagos molinė koncentracija yra 2,00 mol/dm3. Tirpalo tankis 1,13 g/cm3, gliukozės molinė masė 180,12 g/mol.
Sprendimas
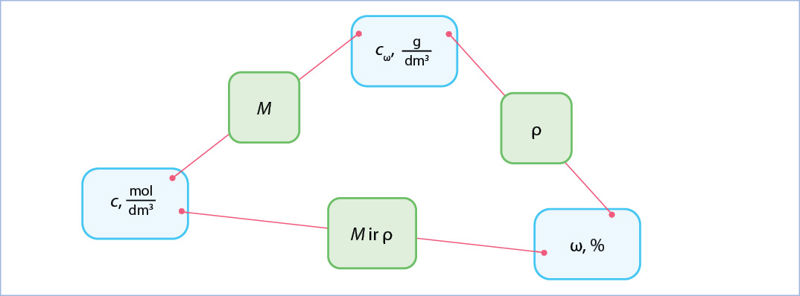
Koncentracijai perskaičiuoti pakanka žinoti tirpalo tankį ρ ir medžiagos molinę masę M (1.5.3 pav.). Pasirenkame skaičiuoti patogų tirpalo mėginį. Duota molinė koncentracija, tad pasirinkę 1 dm3 (t. y. vieną litrą) tirpalo iš karto žinome, kad jame yra 2,00 mol gliukozės. Belieka apskaičiuoti, kokia yra gliukozės masė.
m(gliukozės) = n · M = 2,00 mol · 180,12 g/mol =
360,36 g ≈ 360 g.
Procentinei koncentracijai apskaičiuoti dar reikia sužinoti tirpalo masę. Žinome, kad 1 dm3 = 1000 cm3.
m = ρ · V = 1,13 g/cm3 · 1000 cm3 = 1130 g;
Atsakymas: gliukozės masės koncentracija 360 g/dm3, o procentinė koncentracija 31,9 %.
Klausimai ir užduotys
- Tirpalą sudaro ne mažiau kaip dvi medžiagos. Kaip vadinama kiekviena šių medžiagų?
- Tirpalas yra mišinys. Žinome, kad mišiniai skirstomi į vienalyčius (homogeninius) ir įvairialyčius (heterogeninius). Kuriai mišinių grupei priskiriami tirpalai?
- Apskaičiuokite, kiek gramų natrio chlorido NaCl reikia gaminant 250 cm3 0,025 mol/dm3 šios medžiagos tirpalo?
- Apskaičiuokite tirpalo, kuriame cukraus C12H22O11 molinė koncentracija 0,055 mol/dm3, tūrį. Žinoma, kad tirpalas gautas ištirpinus 5,7 g cukraus.
- Bandymams reikia 0,15 kg tirpalo, kuriame geležies(II) sulfato procentinė koncentracija 8,0 %. Apskaičiuokite tirpalui gaminti reikalingo vandens ir tirpinamosios medžiagos masę, jeigu tirpalas gaminamas iš: a) bevandenio FeSO4 ; b) kristalohidrato FeSO4 · 7H2O.

